
|
|
RADYO ELEKTRONİK VE ELEKTRİK MÜHENDİSLİĞİ ANSİKLOPEDİSİ AA boyutunda galvanik hücrelerin karşılaştırmalı özellikleri. Radyo elektroniği ve elektrik mühendisliği ansiklopedisi
Radyo elektroniği ve elektrik mühendisliği ansiklopedisi / Şarj cihazları, piller, galvanik hücreler Bugün mağazalarda ve pazarlarda birçok farklı galvanik element bulabilirsiniz. Hangilerini seçmeli? Bu makale doğru kararı vermenize yardımcı olacaktır. Galvanik hücreler ve piller çeşitli elektronik ekipmanlara güç sağlamak için yaygın olarak kullanılmaktadır. En yaygın elemanlar AA boyutundadır. Satış raflarında farklı şirketlerin benzer ürünlerini bulabilirsiniz; bunlar çoğunlukla iki elektrokimyasal sistemdir: salin ve alkalin. Energizer yakın zamanda 1,5 V AA boyutlu lityum piller üretmeye başladı. Galvanik hücrenin en önemli özelliği olan kapasite (bir yüke iletebildiği elektrik miktarı) etiket üzerinde neredeyse hiçbir zaman belirtilmez. Alıcılar yalnızca "geleneksel salin hücrelerinden on kat daha uzun süre dayanan" hücreler hakkındaki televizyon reklamlarına güvenebilirler veya Energizer'ın yeni AA boyutlu e2 lityum hücrelerinin geleneksel alkalin hücrelerden beş kat daha uzun süre dayandığına dair sözüne güvenebilirler [1]. Üstelik hangi unsurların “sıradan” olarak adlandırıldığı da tam olarak belli değil. Farklı elektrokimyasal sistemlerin elemanlarının parametrelerini niceliksel olarak karşılaştırmak için bunların aynı koşullar altında test edilmesi gerekir. Bu tür testler üç tip elementle gerçekleştirildi: tuz Philips Long Life ("taze" elementin EMF'si - 1,65 V), alkalin Duracell Ultra MZ (1,62 V) ve lityum Energizer e2 (1,8 V). Her biri, yaklaşık 15 mA'lik bir başlangıç deşarj akımına karşılık gelen 100 ohm'luk bir dirençle yüklendi. Standart boyutlu AA elemanları için bu yük akımı tipiktir. Boşaltma, gerçek çalışma koşullarına karşılık gelen, günde birkaç saatlik döngüler halinde gerçekleştirildi. Bu, Şekil 1'de gösterilen deşarj eğrilerindeki voltaj "sivri uçlarını" açıklamaktadır. XNUMX. Mavi eğri tuz elementine, kırmızı alkalin elemente ve yeşil ise lityum elementine karşılık gelir. "Dinlenme" döneminde, herhangi bir türdeki eleman üzerindeki voltaj biraz arttı, ancak yükü bağladıktan sonra önceki döngüde hızla minimum seviyeye düştü. Noktalar, elemanların EMF değerlerini - yüksüz olarak üzerlerindeki voltajı gösterir.
Bir hücrenin tamamen boşalması için yükteki voltajın 0,9 V'a düşmesini kriter olarak alırsak, tuz hücresinin deneysel olarak belirlenen kapasitesi 1 Ah, alkalin hücresinin 2,9 Ah ve lityum hücresinin 3,5 Ah olduğu ortaya çıkar. . Sonuç olarak, farklı elektrokimyasal sistemlerin elemanlarının kapasitelerindeki beş ve on katlık farklılıklardan bahsetmeye gerek yoktur. İncirde. Şekil 2 başka bir eğri serisini göstermektedir.
Boşalma işlemi sırasında elemanların iç direncinin nasıl değiştiğini gösterirler. Buradaki eleman tipi ve eğri rengi arasındaki yazışma Şekil 1'dekiyle aynıdır. XNUMX. İç direnç R değerleri formül kullanılarak hesaplandı
burada E, elemanın EMF'sidir; U - yük altında voltaj; RH - yük direnci. Deşarj ilerledikçe tuz ve alkali elementlerin iç direnci monoton olarak artar. Ve deşarjın başlangıcında keskin bir şekilde azalan lityum direnci, sonuna kadar neredeyse hiç değişmeden kalır ve ardından aynı keskinlikte artar. Elbette yapılan deneylere kapsamlı denilemez. Bir elemanın kapasitesi kesin olarak sabit bir değer değildir; birçok dış faktöre bağlıdır. Farklı elementler için maksimum değere önemli ölçüde farklı deşarj koşulları altında ulaşılabilir. Bütün bunları hesaba katmak için amatör koşullarda gerçekçi olmayan çok geniş bir dizi deney yapmak gerekli olacaktır. Ancak hesaplamayla elde edilen sonuçları kontrol etmeye çalışalım. Çeşitli elektrokimyasal sistemlerin elementlerinin teorik olarak mümkün olan maksimum kapasitesini tahmin etmek için elektrotlarının, elektrolitlerinin kimyasal bileşimini ve elementte meydana gelen kimyasal reaksiyonu bilmeniz gerekir. Tuz ve alkalin hücreler için katot çinko, anot ise manganez dioksittir. Bu nedenle bu tür elementlere topluca manganez-çinko adı verilir. Ancak içlerindeki elektrolit farklıdır: tuz (genellikle amonyum klorür) veya alkali (potasyum hidroksit). [2]'ye göre reaksiyon manganez-çinko tuzu elementinde meydana gelir.
ve alkalin olarak
Elektrot malzemesi ve lityum hücresindeki kimyasal reaksiyon hakkında güvenilir bilgi yoktur. Yalnızca elektrotların lityum ve manganez dioksit olduğu ve elektrolitin propilen karbonat içindeki bir lityum perklorat çözeltisi olduğu varsayılabilir. Eğer bu tahmin doğruysa [2]'ye göre lityum hücresinde bir reaksiyon meydana gelir.
Faraday yasasını kullanarak galvanik hücre C, Ah'nin kapasitesini belirlemek için bir ifade elde ederiz:
m reaksiyona giren maddelerin kütlesidir F = 96,5-103 C/g-eq - Faraday sayısı; n - değerlik (tuz ve alkalin galvanik hücreler için - 2, lityum için - 1); M reaksiyona giren maddelerin toplam moleküler ağırlığıdır. AA boyutunda galvanik hücreleri tartıyoruz: tuz - 17 g, alkalin - 24 g, lityum - 15 g. Reaksiyona giren maddelerin kütlesi ile hücre gövdesinin kütlesinin ve yer almayan maddelerin kütlesiyle karşılaştırıldığında olduğunu varsayalım. reaksiyonda (karbon elektrot, alkalin ve lityum hücrelerdeki elektrolit) ihmal edilebilir ve ihmal edilebilir. Reaksiyona giren maddelerin toplam moleküler ağırlığını yukarıdaki kimyasal reaksiyon denklemlerinden hesaplıyoruz: tuz için - 346 g, alkalin için - 257 g, lityum için - 94 g Formülde sayısal değerleri değiştirerek mümkün olan maksimum değeri elde ederiz. tuz hücresinin kapasitesi - 2,6 Ah, alkalin - 5 Ah, lityum - 4,3 Ah. Hesaplanan kapasitans değerleri ile ölçülenler arasındaki farklar, hesaplamalarda yapılan oldukça kaba varsayımlarla açıklanabilir. Yani beş ya da on kat fark bulunamadı. Bir alkalin hücrenin teorik kapasitesi, bir tuz hücresinin yaklaşık iki katıdır ve lityumun bu açıdan alkaline göre hiçbir avantajı yoktur. Bu deneysel sonuçlarla tutarlıdır. Yapılan tüm çalışmaların sonuçlarına dayanarak, aşağıdaki sonuçlara varabiliriz: 1. Lityum galvanik hücreler en kararlı voltaja, pratik olarak deşarj derecesine bağlı olmayan en düşük iç dirence ve çok olmasa da en yüksek kapasiteye sahiptir. Tercihen yüksek akım tüketimi olan ekipmanlara ve ayrıca güç kaynağı voltajı düştüğünde otomatik olarak kapanan cihazlara (örneğin dijital kameralar) güç sağlamak için kullanılırlar. 2. Alkalin hücreler, lityumunkiyle karşılaştırılabilir bir kapasiteye sahiptir ve aynı zamanda yüke daha düşük bir voltajda yüksek akım sağlama kapasitesine sahiptir. Otomatik voltaj kontrolü olmayan ortalama akım tüketimine sahip cihazlarda en iyi şekilde kullanılırlar. Çoğu durumda alkalin piller lityum pillere göre tercih edilir çünkü bunlar üç ila dört kat daha ucuzdur. 3. Tuz hücreleri en küçük kapasiteye ve en yüksek iç dirence sahiptir. Düşük akım tüketimi olan ekipmanlarda kullanılması tavsiye edilir. Edebiyat
Yazar: I. Podushkin, Moskova
Dokunma emülasyonu için suni deri
15.04.2024 Petgugu Global kedi kumu
15.04.2024 Bakımlı erkeklerin çekiciliği
14.04.2024
▪ Geri dönüştürülmüş şişelerden yapılmış plastik yol ▪ Armstrong armatürleri için ISSATA LED sürücüleri ▪ Mean Well PSC-160 Güvenlik Güç Kaynakları ▪ Negatif kütleli parçacıklar üreten lazer cihazı
▪ Sitenin Referans materyalleri bölümü. Makale seçimi ▪ makale Ve her yerde ölümcül tutkular ve kaderden korunma yok. Popüler ifade ▪ makale Amerikalılara neden Pindos deniyor? ayrıntılı cevap ▪ kendin yap IrDA makalesi. Radyo elektroniği ve elektrik mühendisliği ansiklopedisi
Makaleyle ilgili yorumlar: konuk Harika bir makale, teşekkürler.
Ana sayfa | Kütüphane | Makaleler | Site haritası | Site incelemeleri www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






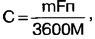
 Bu makaleye yorumunuzu bırakın:
Bu makaleye yorumunuzu bırakın: